Un progetto finanziato dall’associazione di pazienti “CDKL5-Insieme verso la cura” valuterà il ruolo del microbiota, l’insieme dei microrganismi che popolano il nostro intestino, in una rara malattia neurologica, il deficit di CDKL5.

Nel nostro intestino non solo c’è un secondo cervello, ma anche una folta popolazione di microrganismi che vive in simbiosi con noi fin dalle prime fasi della nostra vita, influenzando molte delle nostre funzioni vitali: è il microbiota intestinale, un insieme di batteri, virus, funghi che inizia a formarsi fin dal momento del parto e si arricchisce via via con l’allattamento al seno, poi l’alimentazione e la crescita, stabilizzandosi poi in età adulta quando nel complesso può arrivare fino a 2 kg di peso.
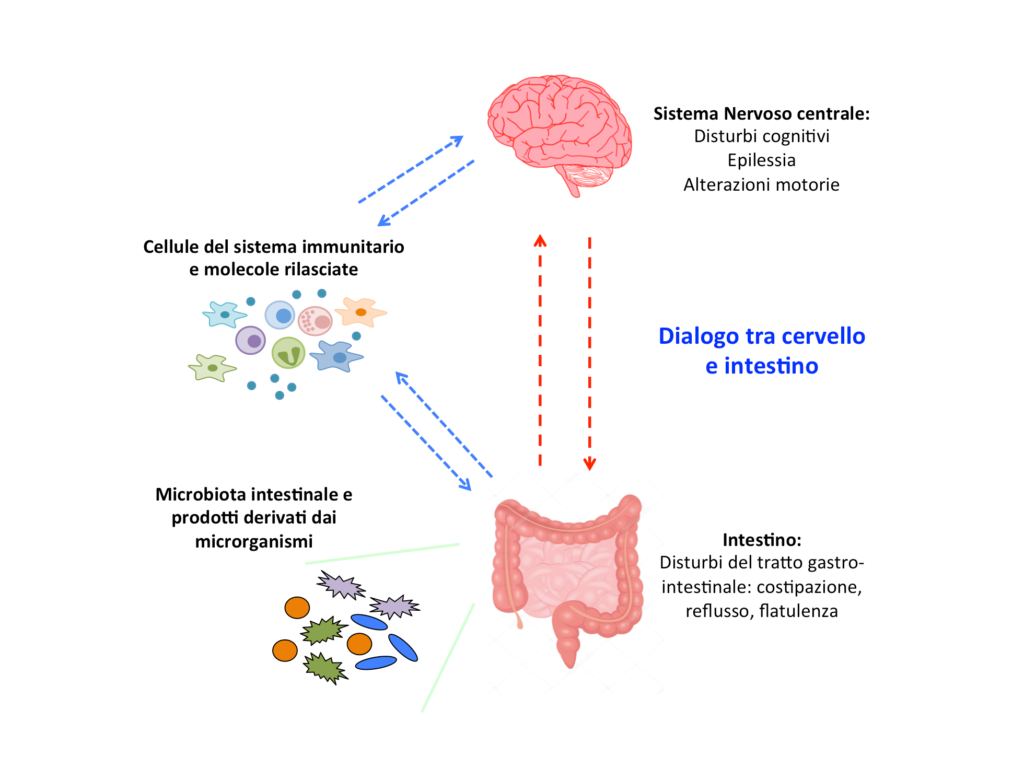
Da oltre 15 anni è noto come questa ricca popolazione che vive in simbiosi con noi non sia a sé stante, ma mantenga un dialogo costante anche con il nostro cervello: studiare il microbiota può rivelarsi quindi una fonte di informazioni preziosa anche per comprendere, e possibilmente correggere, alcune disfunzioni del sistema nervoso.
È quanto si propone di fare Paola Tognini dell’Università di Pisa per una rara malattia genetica del neurosviluppo ad oggi incurabile, il deficit di CDKL5, caratterizzata dalla comparsa, già nelle prime settimane di vita, di manifestazioni epilettiche, riduzione del tono muscolare, problemi alla vista e grave disabilità intellettiva. L’attività elettrica del cervello, sostanzialmente normale all’esordio, si deteriora progressivamente fino a interferire con un normale sviluppo neurologico e cognitivo del bambino.
Grazie a un progetto di durata annuale e del valore di 50mila euro finanziato dall’associazione di pazienti “CDKL5-Insieme verso la cura”, Tognini esplorerà per la prima volta se il microbiota intestinale possa giocare un ruolo nella sintomatologia che si osserva in questi pazienti, un aspetto poco studiato della malattia ma di grande impatto sulla quotidianità delle famiglie.
«Studi condotti sia negli animali che nell’uomo indicano come il microbiota intestinale possa influenzare diverse funzioni del cervello - spiega la ricercatrice - come per esempio la risposta allo stress, il sonno, l’appetito, ma anche del sistema immunitario, che nel corso della vita deve imparare a distinguere i microrganismi utili da quelli invece pericolosi. Inoltre, oggi sappiamo che questa popolazione di microrganismi dialoga costantemente anche con il sistema enterico, il “secondo cervello” presente nel nostro intestino, e può giocare un ruolo nei sintomi gastrointestinali che si possono presentare come co-morbidità in pazienti affetti da disturbi psichiatrici, depressione, malattie neurodegenerative e del neurosviluppo. Per esempio, alcuni studi hanno mostrato come il microbiota di persone con autismo o sindrome di Rett sia diverso da quello dei loro controlli sani, sia in termini di composizione che di produzione di specifici metaboliti: ci siamo quindi chiesti se questo valesse anche per i bambini con deficit di CDKL5».
Grazie anche alla collaborazione con Aglaia Vignoli ed Elisa Borghi dell’Università di Milano, Tognini e il suo gruppo analizzeranno quindi il microbiota di questi pazienti a partire da campioni di feci, così come il cosiddetto “metaboloma”, ovvero l’insieme dei metaboliti e delle varie sostanze, vitamine per esempio, prodotte dai microrganismi intestinali e rilevabili nel sangue, alla ricerca di differenze significative rispetto alle persone sane. Parallelamente, alle famiglie partecipanti sarà chiesto anche di fornire informazioni dettagliate sulla dieta di questi bambini.
«Dobbiamo considerare che il microbiota contribuisce anche a mantenere una barriera al passaggio di sostanze potenzialmente nocive: modifiche nella sua composizione potrebbero alterare la permeabilità dell’intestino a certe sostanze che arrivano così al circolo sanguigno. Questo - continua la ricercatrice - potrebbe spiegare un’altra caratteristica tipica di questi pazienti, ovvero uno stato di infiammazione blanda ma costante, che pur non provocando segni tangibili in certe condizioni potrebbe contribuire alla sintomatologia. Da studi preliminari abbiamo visto che somministrando dei probiotici a topi modello di questa malattia si ottengono dei miglioramenti dal punto di vista comportamentale: grazie a questo progetto vorremmo quindi approfondire se questo legame effettivamente esiste anche nell’uomo».
«Disponendo di dati più solidi potremo capire se intervenendo sulla dieta si possa migliorare la quotidianità di questi bambini in termini di disturbi gastrointestinali, crisi epilettiche, qualità del sonno».
Paola Tognini, ricercatrice Università di Pisa
Inoltre, auspichiamo di individuare dei biomarcatori che possano aiutarci a monitorare la progressione della malattia in modo poco invasivo. Non si tratta certamente di una cura, ma della possibilità di alleviare parte delle difficoltà di ogni giorno di queste famiglie: riuscirci sarebbe davvero gratificante anche per noi».